һ�ָ�ϰ��ѧ��Ӧԭ��----�绯ѧ
ԭ���ԭ����Ӧ��
������˵����
1.����ԭ��صĹ���ԭ����
2.��д�������ļ缫��Ӧ�͵�ط�Ӧ����ʽ��
3.�˽ⳣ���Ļ�ѧ��Դ����ʶ��ѧ��������ת����ʵ�����弰����ҪӦ�á�
4.��ʶ������ʴ��Σ����������������绯ѧ��ʴ��ԭ����ѡ��ǡ���Ĵ�ʩ��ֹ�������Ƚ�����ʴ��
һ��ԭ���
1�����ԭ����ǽ� ��ת��Ϊ �ܵ�װ�á�
2������������
˼���뽻��������װ���У������ԭ��ص�����____________________________
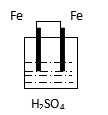
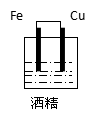
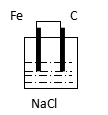
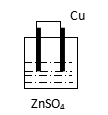


A B C D E F
��1���������ϲ����������ԭ��صĻ�ѧ��Ӧ�ǣ� ��
A��HCl ( aq ) + NaOH ( aq ) = NaCl ( aq ) + H2O ( l ) ��H < 0
B��2CH3OH ( l ) +3O2 ( g ) = 2CO2 ( g ) + 4H2O ( l ) ��H < 0
C��4Fe (OH)2 ( s ) + 2H2O ( l ) + O2 ( g ) = 4Fe (OH)3( s ) ��H < 0
D��2H2 ( g ) + O2 ( g ) = 2H2O ( l ) ��H < 0
��2��ijԭ��ص��ܷ�ӦΪ��2Fe3++Fe == 3Fe2+������ʵ�ָ÷�Ӧ��ԭ�������ǣ� ��
A������Ϊͭ������Ϊ�����������ҺΪFeCl3��Һ
B������Ϊ̼������Ϊ�����������ҺΪFe(NO3)3��Һ
C������Ϊ��������Ϊп���������ҺΪFe2(SO4)3��Һ
D������Ϊ��������Ϊ�����������ҺΪCuSO4��Һ
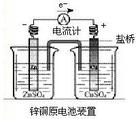 ����ԭ��ع���ԭ��
����ԭ��ع���ԭ��
1������Zn-Cuԭ��أ��ش��������⣺
��ZnSO4��Һ�У�пƬʧȥ���Ӷ��� ���γ�
������Һ�����Ӿ��������� ����Һ�е� �õ��ӱ�
��ԭ�� ����һ�仯���Ա�ʾ���£�
пƬ�� ͭƬ��
˼���뽻�������װ�������ŵ�������ʲô��
2��ԭ����е�ɵ��ƶ�����
���·�� �ڵ�·��
3���缫���ж�
��1�����ݵ缫���ϣ� ��2�����ݵ缫��Ӧ��
��3�����ݵ������������������Һ�������ƶ����� ��4�����ݷ�Ӧ����
��3�����������缫����KOH��Һ�У��������ֱ�ͨ��CH4��O2��������CH4ȼ�ϵ�ء���֪ͨ��CH4��һ������缫��Ӧʽ�ǣ�CH4��10OH����8e��===CO32-��7H2O��ͨ��O2����һ������缫��Ӧ�ǣ�O2��2H2O��4e��===4OH����������������ȷ������ ��
A.ͨ��CH4�ĵ缫Ϊ������ B.��������������Ӧ��
C.ȼ�ϵ�ع���ʱ��Һ�е����������ƶ���D.�õ��ʹ��һ��ʱ���Ӧ����KOH
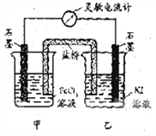 ����߿���1����09�������ۣ������ʺϵ�����������Ӧ2Fe3++2I-=2Fe2++I2��Ƴ�����ͼ��ʾ��ԭ��ء������ж�����ȷ������ ��
����߿���1����09�������ۣ������ʺϵ�����������Ӧ2Fe3++2I-=2Fe2++I2��Ƴ�����ͼ��ʾ��ԭ��ء������ж�����ȷ������ ��
A. ��Ӧ��ʼʱ������ʯī�缫�Ϸ���������Ӧ
B. ��Ӧ��ʼʱ������ʯī�缫��Fe3+����ԭ
C. �����ƶ���Ϊ��ʱ����Ӧ�ﵽ��ѧƽ��״̬
D. �����ƶ���Ϊ����ڼ�����FeCl2����������ʯī�缫Ϊ����
4���缫��Ӧʽ����д��
����߿���2. ���㶫��ѧ14�������ڵ綯��������-����ȼ�ϵ�أ�ͨ����NaCl��Һ��NaOH��ҺΪ���Һ�����Ͻ�Ϊ�����������缫Ϊ����������˵����ȷ���ǣ� ��
A����NaCl��Һ��NaOH��ҺΪ���Һʱ��������Ӧ��Ϊ��O2��2H2O��4e����4OH��
B����NaOH��ҺΪ���Һʱ��������ӦΪ��Al��3OH����3e-��Al(OH)3��
C����NaOH��ҺΪ���Һʱ������ڹ��������е��Һ��pH���ֲ���
D����ع���ʱ������ͨ�����·����������
����߿���3.(���ϻ�ѧ��) ����������ԭ��Ӧ�� 2Ag��(aq)��Cu(s) = Cu2��(aq)��2Ag(s)��Ƶ�ԭ�����ͼ��ʾ��
��ش��������⣺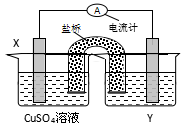
(1)�缫X�IJ�����________���������ҺY��___________��
(2)���缫Ϊ��ص�________���������ĵ缫��ӦΪ______________________________��
X�缫�Ϸ����ĵ缫��ӦΪ____________________________��
(3)���·�еĵ����Ǵ�_______�缫����________�缫��
������ѧ��Դ
1��һ�ε�أ�п�̼��Ե��
�����ɣ����� ������ ���������Һ ��
2�����ε�أ�Ǧ����
����ԭ����
3��ȼ�ϵ�أ�����ȼ�ϵ��
