��II������ѡ���50�֣�
26����������ɸ�������ɺ����ʽ��з��࣬
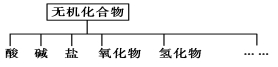
(1)����ͼ��ʾ�����ʷ����������________________��
(2)
|
������� |
�� |
�� |
�� |
������ |
�⻯�� |
|
��ѧʽ |
��HCl ��______ |
��______ ��Ba(OH)2 |
��Na2CO3 ��______ |
��CO2 ��Na2O |
��NH3 ��H2O2 |
��Na��K��H��O��C��S��N���������ֻ�����Ԫ����ɺ��ʵ����ʣ��ֱ���д���ϱ��е��ڢۢ�����ĺ����ϡ�
(3)д����ת��Ϊ���Ļ�ѧ����ʽ��_____________________________________________��
(4)д��ʵ���������Ʊ�O2�Ļ�ѧ����ʽ�� ______________________________________��
(5)ʵ�����Ʊ�������________��________��Ӧ�����������ķ�����
________________________________________________________________________
27����ͼ��һ�ֱ�ʾ���ϵ��ţ���ͼ���������ҷֱ�д��H2O��CO2��Na2O��NaCl��FeCl3�������ʣ�ͼ���������������ʾ��ɹ���Ϊһ�࣬�ཻ����������A��B��C��DΪ����Ӧ�ķ������ݴ��š���ش��������⣺
![]()
(1)�뽫�������ݴ���������Ӧ�������ڣ�
(����)�������ʶ��Ƿǽ���������
(����)�������ʶ����ƵĻ�����
(����)����������һ�������������һ���Ǽ���������
(����)�������ʶ�����
(2)�ýྻ���ձ�ȡ��������ˮ���þƾ��Ƽ��������ڣ����ձ�����μ�����ͼ��ij������M��ˮ��Һ��������п��Ƶ�һ�ֺ��ɫ���塣
������M�Ļ�ѧʽΪ________��
��֤���к��ɫ�������ɵ���õ�ʵ�������________________________________________________________________________
28��2015��9��20���ǵ�27����ȫ������������Ϊ�˷�ֹȣ�ݣ���ȷ��ˢ����ʽ��ѡ�����˵��������Ҫ���������е����ʵ�̽��Ҫ�õ����ѧ֪ʶ��
�±��г������������е�Ħ������
|
���� |
���������� |
���������� |
�������� |
|
Ħ���� |
�������� |
̼��� |
�������� |
(1)���������Ħ�����У������������������̼��ƺͶ�������ֱ���________��________(���������)��
(2)��������Ʋ⣬����Ħ�������ܽ���________(��������������������)��
(3)�����е�Ħ����̼��ƿ�����ʯ��ʯ���Ʊ���ijͬѧ�����һ��ʵ�����Ʊ�̼��Ƶ�ʵ�鷽����������ͼΪ��
�ٸ����ڼ�ˮ�ۼ�Na2CO3��Һ
��д�����������з�Ӧ���Ļ�ѧ����ʽ��
________________________________________________________________________��
29. �����ӵ�����ȡ����ֵ6.02��1023��
(1)2.5 mol Ba(OH)2���____��Ba2��������____��OH����2.5 mol Ba(OH)2��������____g��
(2)0.3 mol NH3����������ԭ������________��H2O����������ԭ������ȡ�
(3)����0.4 mol Al3����Al2(SO4)3������SO4�����ʵ�����________��
(4)��������������6g H2����0.5mol CO2����1.204��1024���Ȼ�����ӣ���147g���ᣬ��92g�Ҵ�(C2H5OH)�����ǵ����ʵ���****����________������������������____________������ԭ�Ӹ���������__________������****����________��
(5)9.5g ij���۽����Ȼ���(ACl2)�к���0.2mol Cl������ACl2��Ħ��������________��A�����ԭ��������________��ACl2�Ļ�ѧʽ��________��
(6) ________������[CO(NH2)2]������Nԭ������10.7g�Ȼ��������Nԭ������ͬ��
30����һ�������������̽������֪1 mol��ͬ�����ڲ�ͬ�����µ������
|
��ѧʽ |
���� |
1 mol �������/L |
|
H2 |
0 ����101 kPa |
22.4 |
|
O2 |
0 ����101 kPa |
22.4 |
|
CO |
0 ����101 kPa |
22.4 |
|
H2 |
0 ����202 kPa |
11.2 |
|
CO2 |
0 ����202 kPa |
11.2 |
|
N2 |
273 ����202 kPa |
22.4 |
|
NH3 |
273 ����202 kPa |
22.4 |
(1) ���ϱ������ó��Ľ��ۣ�
��1 mol�κ����壬�ڱ�״���µ������ԼΪ________��
��1 mol��ͬ�����壬�ڲ�ͬ�������£����____________(����һ��������һ������������һ����)��ȡ�
(2) �������ݣ���ͬ�����£�1 mol�κ���������������ȣ�ԭ���ǣ���__________________��
��__________________________��
(3) Ӧ�ã��ڱ�״���£�4 g O2�����Ϊ__________________��
(4) ���¡���ѹ�£��������O2��O3�������Ӹ�����______��������Ϊ_______��
(5) ��֪16 g A��20 g Bǡ��****��Ӧ����0.04 mol C��31.76 g D����C��Ħ������Ϊ_____��
�������ܱ������зֱ����Ne��H2��O2�������壬�����ǵ��¶Ⱥ��ܶȶ���ͬʱ�������������ѹǿ(p)�ֱ���p(Ne)��p(H2)��p(O2)��ʾ���ɴ�С��˳����____________��
