��һ��ѧ����
���Ծ���Ϊ�����(ѡ����)�͵ڢ��(��ѡ����)�����֣���7ҳ������100�֣�����ʱ��90���ӡ�
�����õ������ԭ��������H��1��C��12 N��14�� O��16�� S��32 Cl��35.5
Na��23 Mg��24 Mn��55 k��39
�����(ѡ��������44��)
һ������ѡ���⣺�������ֹ�22С�⣬ÿС��2�֣���44����
1�������ǵ��ճ������г��������ӵ�ʳ�Ρ������������͡������߸�ţ�̡�����������Ҷ���͡��������ࡱ����Ʒ������ĵ⡢�����ơ�������Ӧ����Ϊ( )
A��Ԫ�� B������
C������ D��������
2���������ʵķ������ȫ����ȷ���ǣ� ��
|
���� |
ǿ����� |
������� |
�ǵ���� |
|
A |
NaCl |
H2O |
Cl2 |
|
B |
H2SO4 |
CaCO3 |
CCl4 |
|
C |
AgCl |
HClO |
Cu |
|
D |
Ba(OH)2 |
H2S |
C2H5OH |
3���������ʵ��������仯ѧʽ����;���������( )
A���ռNa2CO3���Ʋ��� B��С�մ�NaHCO3������θ�����
C���մ�NaOH����ֽ D��ʳ�Ρ�NaCl������
4���飨Bi����ҽҩ��������ҪӦ�������й���![]() Bi��
Bi��![]() Bi��˵����ȷ���ǣ�����
Bi��˵����ȷ���ǣ�����
A��![]() Bi��
Bi��![]() Bi������83������
Bi������83������
B��![]() Bi��
Bi��![]() Bi��Ϊͬλ��
Bi��Ϊͬλ��
C��![]() Bi��
Bi��![]() Bi�ĺ����������ͬ
Bi�ĺ����������ͬ
D��![]() Bi��
Bi��![]() Bi�ֱ���126��127������
Bi�ֱ���126��127������
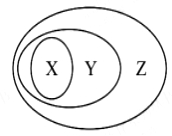 5. ��ͼ����ʾ��һЩ���ʻ�����Ĵ�����ϵ����ȷ����( )
5. ��ͼ����ʾ��һЩ���ʻ�����Ĵ�����ϵ����ȷ����( )
|
|
X |
Y |
Z |
|
A |
�ɱ� |
������ |
������ |
|
B |
��ˮ����� |
����� |
������ |
|
C |
������Һ |
���� |
��ɢϵ |
|
D |
�û���Ӧ |
������ԭ��Ӧ |
���ӷ�Ӧ |
6������ͬ����������NaHCO3��ĩ����һ�ݼ����������ᣬ�ʶ����ȼ���ʹ��
****�ֽ��ټ�����ͬ�������������ᣬ�����������ĵ��������Ȼ����������
�� ��
A��2:1 B��1:1 C��1:2 D��4:2
7����ͼ��ʾ�����ر�������һ�ֺ������������徭����ƿ��ͨ
����ƿ����������ɫ�����ر�����ͨ���������壬������ɫ��
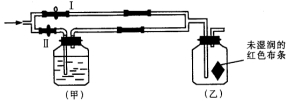 ��ƿ����ʢ���Լ����ܣ� ��
��ƿ����ʢ���Լ����ܣ� ��
��ŨH2SO4 ��NaOH��Һ
��KI��Һ �ܱ���NaCl��Һ
A���� B���ڢ�
C���٢ڢۡ��� D���٢ڢ�
8�����и������ʼ�ķ�Ӧ������������ԭ��Ӧ�����������ӷ�Ӧ����(�� ��)
A��Zn��ϡH2SO4
B��NaCl��Һ��AgNO3��Һ
C��H2��O2
D��Na2O��H2O
9������������ȷ����( )
A��1molH2O������Ϊ18g/mol
B����״���£�1mol�κ����������Ϊ22.4L
C��CH4��Ħ������Ϊ16g
D��3.01��1023��SO2���ӵ�����Ϊ32g
10������ijЩ���ӵļ��鼰������ȷ����( )
A����������ɫ�����������������ʹ����ʯ��ˮ�����ǣ�ԭ��Һ��һ����CO32��
B���Ȼ�����Һ�а�ɫ�����������ټ����ᣬ��������ʧ��ԭ��Һ��һ����SO42��
Cij��Һ����ɫ��ӦΪ��ɫ�������Һ��һ����Na+
Dij��Һ�м���Na2CO3��Һ���а�ɫ�����������Һ��һ����Ca2+
11����NA��ʾ�����ӵ���������ֵ������˵����ȷ����( )
A��1molCl2������������Ӧת�Ƶĵ�������2NA
B�����³�ѹ��22.4L HCl���庬�еķ�������NA
C��0.1mol/L CuCl2��Һ��Cl����Ŀ��0.2NA
D��32gO2�к��е�ԭ������NA
12���������������ʻ���;��������������ʵ����( )
A����ˮ����Ư�ױ�����HClO��ǿ������
B����һС�������Ͷ��ϡ����ͭ��Һ�л��к�ɫ��������
C���������ƿ�������������еĹ�����
D����������Na2CO3��NaHCO3���ֹ��壬�ֱ���������ᷴӦ��NaHCO3����CO2�������Ƚ϶�
13�����з�Ӧ�����ӷ���ʽ��д��ȷ����( )
A��п����ϡ���ᷴӦ��Zn+2H+=Zn2++H2��
B���廯����Һ��������Ӧ��Br��+Cl2=Cl��+Br2
C��������ͭ��ϡ���ᷴӦ��OH��+H+=H2O
D������ˮ��Ӧ��Na++2H2O=Na++2OH��+H2��
14����ˮ��һ����Ļ�ѧ��Դ�⣬�����йغ�ˮ�ۺ����õ�˵����ȷ����( )
A�����ó�ϫ�����ǽ���ѧ��ת��Ϊ����
B����ˮ�����ƺ��εĹ�����ֻ�����˻�ѧ�仯
C���Ӻ�ˮ�п��Եõ�NaCl���������NaCl���Ʊ�Na
D����ˮ�к�����Ԫ�أ�ֻ�辭�������仯�Ϳ��Եõ��嵥��
15�����б仯�����������������ʵ�ֵ��ǣ� ����
A�� Cl-��Cl2 B��Fe3+��Fe2+ C��CuO��Cu D H2SO4��BaSO4
16.���п��Դ�����������Һ����ɫ���������ǣ� ����
A��H+��Na+��NO3����Cu2�� B��Ba2+��Mg2+��Cl����SO42��
C��H+��K+��OH����NO3- D��NO3����SO42����K+��Mg2+
17��ȼ�ŵ�þ�������������в��ܼ���ȼ�յ��ǣ� ��
A��CO2 B��N2 C��Cl2 D��He
18��������������������ȷ���� ( )
A����ɫʳƷ�Dz����κλ�ѧ���ʵ�ʳƷ
B���ӵ�ʳ�������ӵġ��⡱һ���ǵ⻯����ⵥ��
C�������Ȼ�����Һ������������������ö����ЧӦ
D���ø������ɫ�������Լ����Ȼ����������Ƿ��������
19����xR2++yH++O2=4R3++nH2O�����ӷ���ʽ�У������ж���ȷ���� �� ��
A. y=4��R2+�������� B. y=2��R2+�ǻ�ԭ��
C. y=2��R3+�ǻ�ԭ���� D. y=4��R3+����������
20. ���µ��뷽��ʽ�������( )
A��MgCl2��Mg2++2Cl�� B��Fe2(SO4)3��2Fe3++3SO42��
C��NaHCO3��Na++H++CO32�� D��NaOH��Na++OH��
21��ijԪ���ڻ�ѧ��Ӧ���ɻ���̬��Ϊ����̬�����Ԫ�أ� ��
A��һ������ԭ�� B��һ����������
C���ȿ��ܱ�����Ҳ���ܱ���ԭ D���Ȳ����ܱ�������Ҳ�����ܱ���ԭ
22������KI��NaBr�Ļ����Һ��ͨ�������Cl2��ַ�Ӧ������Һ���ɲ�����,���ʣ��Ĺ���������( )
A��KI��NaBr B��KCl��NaCl C��KCl��NaBr D��KCl��NaCl��I2
���������ѡ���⣬��56�֣�
23������⣨ÿ��1�֣���8�֣�
�����������ʣ���̼������ �������� ��SO2 ���� ������ ���������� ��������H2SO4�������Ҵ� �뽫�������ʰ�����Ҫ����࣬�������������հ״���
(1)����ɷ��࣬���ڵ��ʵ���____�������������������____�����ڼ������������____�����������____�����ڼ����____�������ε���____��
(2)���Ƿ��ǵ���ʷ��࣬���ڵ���ʵ���____�����ڷǵ���ʵ���____��
24��ÿ��2�֣���10�֣�
��1��0.3mol NH3����������ԭ������____��H2O����������ԭ������ȣ�
��2����0.4mol A13+��Al2��SO4��3��������SO42�������ʵ�����____��
��3����֪16g A��20g Bǡ��****��Ӧ����0.04mol C��31.76g D����C��Ħ������Ϊ____��
��4����һ�����¶Ⱥ�ѹǿ�£�1�������X2��3�������Y2��������2����������û�����Ļ�ѧʽ��____��
��5��ij�λ����Һ�к������ӣ�Na+��Mg2+��Cl����SO42�������Na+��Mg2+ ��
Cl�������ʵ���Ũ������Ϊ��0.2mol•L��1��0.25mol•L��1��0.4mol•L��1��
��c��SO42����=____��
25����ÿ��1�֣���7�֣���ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺
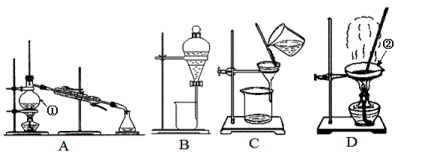
��1��װ��A�������ٵ�������_____________��
װ��D�������ڵ�������_____________��
��2�����Ȼ�����Һ�еõ��Ȼ��ع���,Ӧѡ��װ��_____�������װ��ͼ����ĸ����ͬ�����ӵ�ˮ�з����I2��ѡ��װ��____����װ�õ���Ҫ����������____�����뱥��ʳ��ˮ��ɳ�ӵĻ���Ӧѡ��װ��____���������Ȼ�̼���е�Ϊ76.75�棩�ͼױ���110.6�棩�Ļ���Ӧѡ��װ��____��
26����12�֣�ʵ���ҿ����ø�����غ�Ũ���ᷴӦ��ȡ������Cl2������Ӧ�Ļ�ѧ����ʽ���£�
2KMnO4+16HCl��Ũ����2KCl+2MnCl2+5Cl2��+8H2O
��1��Ũ�����ڷ�Ӧ�����ֳ�____����____��. ����2�֣�
��2��KMnO4�������Ա�Cl2��������____��ѡ����ǿ������������ ��1�֣�
��3������Ӧ��ת����2mol����ʱ����____mol HCl�μӷ�Ӧ����____mol HCl������������Cl2�ڱ�״�������Ϊ____L��
��4��ijͬѧ����KMnO4��������90mL 0.5mol/L����Һ���ش��������⣺
������KMnO4��Һʱ���õ���Ҫ������������ƽ��ҩ�ס��ձ�������������Ͳ��
_________________������ȱ�ٵ��������м���д������
��Ӧ��������ƽ��ȡKMnO4����____g��
�۲��淶��ʵ������ᵼ��ʵ�����������в����ᵼ��������ҺŨ��ƫ�͵���____��
A����ˮ����ʱ���ӿ̶���B������ƿ�ڱڸ���ˮ���δ���ﴦ��
C���ߵ�ҡ�Ⱥ��ְ�Һ����ڿ̶����ּ�ˮ����
D�����ܽ������������Һ�彦���ձ���