ΡΤΦΑΤδΜ·ΚœΈο
ΑύΦΕΘΚ –’ΟϊΘΚ ―ßΚ≈ΘΚ
“ΜΓΔΟς»ΖΡΩ±ξΘ§Ή‘÷ς―ßœΑ
1. ΫΧ―ßΡΩ±ξΘΚ
Θ®1Θ©ΙΊΉΔΡΤΒ»ΦΑΤδ÷Ί“ΣΜ·ΚœΈο‘Ύ…ζ≤ζΓΔ…ζΜν÷–ΒΡ”Π”Ο ΒάΐΘ§Ά®ΙΐΤδ–‘÷ ΒΡ Β―ιΧΫΨΩΘ§‘ω«Ω―ßœΑΜ·―ßΒΡ–Υ»ΛΘ§≈ύ―χΩΤ―ßΧΫΨΩΡήΝΠ
Θ®2Θ©ΝΥΫβΡΤΦΑΤδ÷Ί“ΣΜ·ΚœΈοΒΡ÷ς“ΣΈοάμΓΔΜ·―ß–‘÷ Θ§±»ΫœNa2CO3ΓΔNaHCO3 ΒΡ»ήΫβ–‘ΓΔ»»Έ»Ε®–‘ΓΔ”κΥαΖ¥”Π
Θ®3Θ©≥θ≤Ϋ―ßΜαΦχ±πNa2CO3ΓΔNaHCO3ΒΡΖΫΖ®
Θ®4Θ©ΝΥΫβΡΤΓΔΦΊΒΡ―φ…ΪΖ¥”Π
2. ‘ΛœΑΡΎ»ίΘΚ
“ΜΓΔΡΤ
1Θ°ΡΤΒΡΈοάμ–‘÷
―’…ΪΘΚ Θ§”–Ϋπ τΙβ‘σΘΜΟήΕ»ΘΚΠ―(H2O) Π―(Na) Π―(ΟΚ”Ά)ΘΜ
»έΒψΘΚ 100 ΓφΘΜ”≤Ε»ΘΚ÷ ΒΊ Θ§Ω…“‘”Ο–ΓΒΕ«–ΗνΓΘ
2Θ°ΡΤΜ·―ß–‘÷
(1)”κΖ«Ϋπ τΒΞ÷ (»γO2ΓΔCl2)ΒΡΖ¥”Π
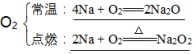
Cl2ΘΚ
(2)”κΥ°Ζ¥”Π
ΔΌάκΉ”ΖΫ≥Χ ΫΘΚ ΓΘ
ΔΎ”κΒΈΦ”Ζ”ΧΣΒΡΥ°Ζ¥”ΠΒΡœ÷œσΦΑΫβ Ά

(3)”κ―ΈΥαΖ¥”Π
άκΉ”ΖΫ≥Χ ΫΘΚ ΓΘ
3Θ°ΡΤΒΡ÷Τ»ΓΦΑ±Θ¥φ
(1)÷Τ»ΓΘΚΜ·―ßΖΫ≥Χ ΫΈΣ ΓΘ
(2)±Θ¥φΘΚΟήΖβ±Θ¥φΘ§Ά®≥Θ±Θ¥φ‘Ύ ΓΘ
4Θ°ΡΤΒΡ”ΟΆΨ
(1)÷Τ»ΓNa2O2Β»Μ·ΚœΈοΓΘ
(2)ΡΤΓΔΦΊΚœΫπ(“ΚΧ§)Ω…”Ο”Ύ‘≠Ή”Ζ¥”ΠΕ―ΒΡΒΦ»»ΦΝΓΘ
(3)”ΟΉςΒγΙβ‘¥Θ§÷ΤΉς ΓΘ
(4)“±ΝΕΡ≥–©Ϋπ τΘ§Ϋπ τΡΤΨΏ”–«ΩΒΡΜΙ‘≠–‘Θ§»έ»ΎΉ¥Χ§œ¬Ω…“‘”Ο”Ύ÷Τ»ΓΫπ τΘ§»γ4NaΘΪTiCl4»έ»Ύ4NaClΘΪTiΓΘ
ΕΰΓΔΙΐ―θΜ·ΡΤ”κΙΐ―θΜ·ΡΤ
|
Μ·―ß Ϋ |
Na2O |
Na2O2 |
|
―θ‘ΣΥΊΜ·ΚœΦέ |
|
|
|
…ΪΓΔΧ§ |
|
|
|
“θΓΔ―τάκΉ”Ηω ΐ±» |
|
|
|
”κΥ°Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ |
|
|
|
”κCO2Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ |
|
|
»ΐΓΔΧΦΥαΡΤ”κΧΦΥα«βΡΤ
1Θ°–‘÷ ”κ±»Ϋœ
|
Na2CO3 |
NaHCO3 |
–‘÷ ±»Ϋœ | |
|
Υ°»ή–‘ |
|
|
œύΆ§Έ¬Ε»œ¬Θ§Na2CO3ΒΡ»ήΫβΕ» ”ΎNaHCO3 |
|
”κCaCl2Ζ¥”Π |
|
|
CaCl2+Na2CO3= |
|
”κCa(OH)2Ζ¥”Π |
|
|
Ca(OH)2+ Na2CO3= Ca(OH)2+ NaHCO3= |
|
”κΥαΖ¥”Π |
|
|
ΕΦΖ≈≥ω NaHCO3”κΥαΖ¥”ΠΒΡΨγΝ“≥ΧΕ»«Ω”ΎNa2CO3 |
|
»ή“ΚΒΡΥαΦν–‘ |
|
|
Έο÷ ΒΡΝΩ≈®Ε»œύΆ§ ±Θ§Na2CO3»ή“ΚΒΡpH±» NaHCO3»ή“ΚΒΡ |
|
»»Έ»Ε®–‘ |
|
|
2NaHCO3 |
2Θ°ΉΣΜ·
Na2CO3![]() NaHCO3
NaHCO3
ΥΡΓΔNa+ΓΔK+ΒΡΦλ―ι
1.Η≈ΡνΘΚΡ≥–©Ϋπ τΜρΥϋΟ«ΒΡΜ·ΚœΈο‘ΎΉΤ…’ ±ΕΦΜα ΙΜπ―φ≥ œ÷≥ωΧΊ βΒΡ―’…ΪΘ§
Τδ τ”ΎΈοάμ±δΜ·Θ§ τ”Ύ‘ΣΥΊΒΡ–‘÷ ΓΘ
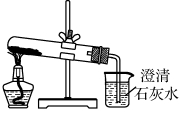
2.―φ…ΪΖ¥”ΠΒΡ≤ΌΉς
≤§ΥΩΨΤΨΪΒΤΈό…Ϊ¥ΐ≤βΈοΨΤΨΪΒΤΙέ≤λΜπ―φ―’…Ϊ”Ο―ΈΥα≤§ΥΩΨΤΨΪΒΤΈό…Ϊ
3.≥ΘΦϊ‘ΣΥΊΒΡ―φ…Ϊ
ΡΤ‘ΣΥΊ …ΪΘΜ
ΦΊ‘ΣΥΊ …Ϊ(ΆΗΙΐάΕ…Ϊνή≤ΘΝßΙέ≤λ).
ΕΰΓΔΚœΉς Ά“…Θ§ΜΞœύ―–Χ÷
ΧΫΨΩ“ΜΘΚ±»ΫœΫπ τΡΤΖ÷±π”κΥ°ΓΔ―ΈΥαΚΆΝρΥαΆ≠»ή“ΚΒΡΖ¥”ΠΓΘ
ΧΫΨΩΕΰΘΚ±»Ϋœ―θΜ·ΡΤ”κΙΐ―θΜ·ΡΤΒΡ“λΆ§ΒψΓΘ
ΧΫΨΩ»ΐΘΚ±»ΫœΧΦΥαΡΤ”κΧΦΥα«βΡΤΒΡ“λΆ§ΒψΓΘ
»ΐΓΔΨΪ–ΡΒψ≤ΠΘ§ΤτΖΔ“ΐΒΦ
άΐ1 œ¬ΟφΙΊ”ΎΫπ τΡΤΒΡΟη ω≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A.ΡΤΒΡΜ·―ß–‘÷ ΚήΜνΤΟΘ§‘ΎΉ‘»ΜΫγάο≤ΜΡή“‘”ΈάκΧ§¥φ‘Ύ
B.ΡΤάκΉ”ΚΆΫπ τΡΤΉΤ…’Μπ―φΕΦ≥ ΜΤ…Ϊ
C.ΡΤΡήΑ―ν―ο·Β»Ϋπ τ¥”ΥϋΟ«ΒΡ―Έ»ή“Κ÷–ΜΙ‘≠≥ωά¥
D.ΡΤΚΆΦΊΒΡΚœΫπ‘Ύ “Έ¬œ¬≥ “ΚΧ§Θ§Ω…Ής‘≠Ή”Ζ¥”ΠΕ―ΒΡΒΦ»»ΦΝ
άΐ2 œ¬Ν–ΙΊ”ΎNa2CO3ΒΡ–π ω÷–Θ§≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ)
AΘ°Υ°»ή“Κœ‘Υα–‘ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
BΘ°÷ΈΝΤΈΗΥαΙΐΕύΒΡ“Μ÷÷“©ΦΝ
CΘ°»»ΒΡNa2CO3»ή“ΚΩ…”Οά¥≥ΐ»Ξ’¥ΈέΓΓΓΓΓΓΓΓ
DΘ°œρΧΦΥα±ΞΚΆ»ή“Κ÷–Ά®»κΙΐΝΩCO2ΤχΧεΘ§»ή“ΚΜα≥ωœ÷ΜκΉ«
άΐ3 (2016Ϋλ―ο÷ί –ΡΘΡβ“Μ)œ¬Ν–ΙΊ”ΎNa2CO3ΚΆNaHCO3ΒΡΥΒΖ®÷–≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ)
A. Ω…”Ο≥Έ«ε ·Μ“Υ°Φχ±π’βΝΫ÷÷Έο÷
B. Na2CO3±»NaHCO3ΗϋΈ»Ε®
C. œύΆ§ΧθΦΰœ¬Έο÷ ΒΡΝΩ≈®Ε»ΨυΈΣ0.5 mol/LΒΡNa2CO3»ή“ΚΒΡΦν–‘±»NaHCO3»ή“Κ«Ω
D. Β»Έο÷ ΒΡΝΩΒΡNa2CO3ΚΆNaHCO3”κΉψΝΩ―ΈΥαΖ¥”Π…ζ≥…ΒΡΕΰ―θΜ·ΧΦ÷ ΝΩœύΒ»
ΥΡΓΔΙ°ΙΧ―ΒΝΖΘ§Χα…ΐΦΦΡή
1Θ° ΓΑΫ≈”ΓΓ±ΓΔΓΑ–ΠΝ≥Γ±ΓΔΓΑΈεΜΖΓ±Β»―φΜπ»Ο±±Ψ©Α¬‘ΥΜαΩΣΡΜ ΫΗϋΦ”Μ‘ΜΆΉ≥ΙέΘ§’β–©Έε≤ γΆΖΉΒΡ―φΜπ”κ‘ΣΥΊΒΡ―φ…ΪΖ¥”Π”–ΙΊΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «
AΘ°Ιέ≤λK2SO4ΒΡ―φ…Ϊ”ΠΆΗΙΐάΕ…ΪΒΡνή≤ΘΝß
BΘ°Na”κNaCl‘ΎΉΤ…’ ±Μπ―φ―’…ΪœύΆ§
CΘ°Ω…“‘”Ο―φ…ΪΖ¥”Πά¥«χ±πNaClΚΆKCl
DΘ°―φ…ΪΖ¥”Π“ΜΕ®ΖΔ…ζΜ·―ß±δΜ·
2.ΫΪœ¬Ν–ΙΧΧεΆΕ»κ ΝΩΥ°÷–Θ§‘ΌΒΈΦ”Ζ”ΧΣΘ§»ή“Κ≤ΜΜα±δΈΣΚλ…ΪΒΡ «(ΓΓΓΓ)
A. Na B. Na2O C. Na2CO3 D. NaCl
3.œ¬Ν–”–ΙΊNa2CO3ΚΆNaHCO3ΒΡΥΒΖ®÷–Θ§’ΐ»ΖΒΡ «(ΓΓΓΓ)
A. »»Έ»Ε®–‘ΘΚNa2CO3ΘΦNaHCO3
B. œύΆ§Έ¬Ε»œ¬‘ΎΥ°÷–ΒΡ»ήΫβΕ»ΘΚ Na2CO3ΘΦNaHCO3
C. Β»÷ ΝΩΒΡΝΫ÷÷ΙΧΧεΘ§Ζ÷±π”κΙΐΝΩ―ΈΥαΖ¥”ΠΘ§…ζ≥…CO2ΒΡ÷ ΝΩœύΒ»
D. »Γ1 molΓΛLΘ≠1ΒΡΝΫ÷÷»ή“ΚΘ§Ζ÷±πΒΈ»κΖ”ΧΣΘ§»ή“Κ―’…ΪΫœ…νΒΡ «Na2CO3»ή“Κ
4. (2015ΡξΡΨδ¬ΗΏΦΕΡΘΡβ)…ηΦΤœ¬Ν– Β―ιΖΫΑΗΦχ±πNa2CO3ΚΆNaHCO3ΝΫ÷÷ΑΉ…ΪΖέΡ©Θ§≤ΜΡή¥οΒΫ‘ΛΤΎΡΩΒΡΒΡ «(ΓΓΓΓ)
A. Ζ÷±πœρΒ»÷ ΝΩΒΡΑΉ…ΪΖέΡ©÷–Φ”Β»ΧεΜΐΓΔΒ»≈®Ε»ΒΡœΓ―ΈΥαΘ§±»Ϋœ…ζ≥…ΤχΧεΒΡΩλ¬ΐ
B. Ζ÷±πœρΒ»÷ ΝΩΒΡΑΉ…ΪΖέΡ©÷–Φ”Β»ΧεΜΐ ΝΩΒΡΥ°Θ§±»ΫœΙΧΧε»ήΫβΝΩΒΡΕύ…Ό
C. Ζ÷±πΫΪΒ»÷ ΝΩΒΡΑΉ…ΪΖέΡ©≈δ≥…»ή“ΚΘ§»ΜΚσΦ”»κ≥Έ«ε ·Μ“Υ°Θ§±»Ϋœ «Ζώ”–≥ΝΒμ…ζ≥…
D. Ζ÷±πΫΪΒ»÷ ΝΩΒΡΑΉ…ΪΖέΡ©”Ο”“ΆΦΉΑ÷ΟΫχ–– Β―ιΘ§±»Ϋœ≥Έ«ε ·Μ“Υ° «Ζώ±δΜκΉ«
5. (2015ΡξΫ≠Υ’ ΓΈΐ…ΫΗΏΦΕΡΘΡβ)Φ”»»¥ΩΦνΚΆ–ΓΥ’¥ρΒΡΜλΚœΈο20gΘ§÷Ν÷ ΝΩ≤Μ‘Ό±δΜ·ΈΣ÷ΙΘ§ά以Κσ≥ΤΝΩΤδΙΧΧε÷ ΝΩ «13.8gΘ§‘ρ‘≠ΜλΚœΈο÷–¥ΩΦνΒΡ÷ ΝΩΖ÷ ΐ «(ΓΓΓΓ)
A. 84% B. 8.4% C. 1.6% D. 16%
ΈεΓΔΖ¥ΥΦΉήΫαΘ§ΙΙΫ®÷ΣΆχ
Έ“ΒΡάßΜσΘΚ
Έ“ΒΡ ’ΜώΘΚ
ΝυΓΔΉς“Β
ΩΈ ±Ής“Β ΒΎ6ΩΈ ± ±ΊΉωΧβ1-6ΓΔ8-11Θ§―ΓΉωΧβ7ΓΔ12
‘ΛœΑΉς“Β ¬ΝΦΑΤδΜ·ΚœΈο
―ß–ΘΉ…―·¥ΠΘΚ±ΘΕ® –ΨΚ–ψ«χΤΏ“Μ÷–¬Ζ1317Κ≈ Ή…―·ΒγΜΑΘΚ0312-4442550
¥όάœ ΠΘΚ15350617957Θ®Ά§ΈΔ–≈Θ© ΗΏάœ ΠΘΚ19213065640Θ®Ά§ΈΔ–≈Θ©
≥¬άœ ΠΘΚ13833233159Θ®Ά§ΈΔ–≈Θ© Ήφάœ ΠΘΚ19213027557Θ®Ά§ΈΔ–≈Θ©
ICP±ΗΑΗΚ≈ΘΚΦΫICP±Η17032056Κ≈-1
