�ڶ���![]() �л�������Ľṹ�ص�
�л�������Ľṹ�ص�
![]()
���α�Ҫ��
1��֪�������л�������Ľṹ��
2��ͨ���Ե���ʵ���ķ������˽��л�����������칹�������жϼ��л��������ͬ���칹�塣
�����
1.��ȷ���ýṹʽ���ṹ��ʽ������ʽ������ʽ�Ȼ�ѧ�����ʾ�����л���Ľṹ����ʶ���ģ�ͺͱ���ģ�͡�
2���ܱ��ͬ���칹�壬������д�л���ͬ���칹��Ľṹ��ʽ��
3����ȷͬ���칹����칹��ʽ��λ���칹��̼���칹���������칹��
����ѧ��λ
���ʵĽṹ�������ʵ����ʣ����ʵ����ʷ�ӳ���ʵĽṹ������ʱ�����л�����ԭ�ӵijɼ��ص㼰ͬ���칹���ᴩ�ں�������ͬϵ���ѧϰ�У������л��ﷴӦʱ�ɼ����ϼ����ɺ�ͬ���칹����жϼ���д�Ǹ߿������еıؿ��㡣
![]()
���¿ε��뽨��
��Ȼ̼Ԫ���ڵؿ��еĺ����ϵ͡�����̼�����������ȴ�쳣�࣬�ֲ�Ҳʮ�ֹ㷺�����������������ռ��������������л������Ŀǰ������Ȼ���з��ֵĺ����˹��ϳɵ��л��������Ѿ��м�ǧ���֣������µ��л����������ڲ��ϵر����ֻ�ϳɳ�����Ϊʲô�л����������˷����أ�
|
�л���������̼ԭ�ӵijɼ��ص� |
1.̼ԭ�ӵijɼ��ص�
(1)̼ԭ���������4�����ӣ�������ԭ���γ�4�����ۼ���
(2)̼̼֮��Ľ�Ϸ�ʽ�е�����˫����������
(3)���̼ԭ�ӿ������ϳ�̼����Ҳ���Խ�ϳ�̼�������Դ���֧����
2������ķ��ӽṹ
|
����ʽ |
�ṹʽ |
����ʽ |
�ռ乹�� |
�ṹʾ��ͼ |
|
|
CH4 |
CHHHH |
H��CH |
�aH ��H |
�������� |
|
��ǰ����
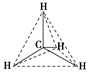
1����������4��̼����ļ����ͼ��ܾ���ͬ���ܷ�˵��������Ӳ���ƽ��ṹ��
����ʾ�������ܡ����������Ϊƽ��ṹ��4��̼���Ҳ���Ե�ͬ��
|
�л��������ͬ���칹���� |
1.ͬ���칹����
�����������ͬ�ķ���ʽ�������в�ͬ�ṹ������
2��ͬ���칹��
����ͬ���칹����Ļ����ﻥΪͬ���칹�壬���ص��Ƿ���ʽ��ͬ���ṹʽ��ͬ���������ʲ�ͬ��
3������ͬ���칹����
|
�칹��� |
�γɷ�ʽ |
ʾ�� |
|
̼���칹 |
̼���Ǽܲ�ͬ���������칹 |
CH2===CH��CH2CH3�� |
|
CCH3CH3CH2 |
||
|
λ���칹 |
������λ�ò�ͬ���������칹 |
CH2===CH��CH2CH3�� |
|
CH3CH===CHCH3 |
||
|
������ |
||
|
�칹 |
���������ͬ���������칹 |
CH3CH2OH�� |
|
CH3��O��CH3 |
��ǰ˼��
2����Է���������ȵIJ�ͬ����һ����Ϊͬ���칹����
����ʾ������һ������Է���������ȵIJ�ͬ���ʿ��ܾ��в�ͬ�ķ���ʽ����CH3COOH��CH3CH2CH2OH��H2SO4��H3PO4��CH2===CH2��CO��N2�ȡ�
|
�л�����ӽṹ�ı�ʾ���� |
�����˼����
����ʾ�л�����ӽṹ����ɵķ�������Щ��
����ʾ��������ʽ�����ʽ������ʽ���ṹʽ���ṹ��ʽ�����ģ�͡�����ģ�͡�����ʽ��
����ʾ�л�����ӿռ乹�͵ķ�������Щ��
����ʾ��������ģ�ͺ����ģ�͡�
|
���� |
��ʾ���� |
ʵ�� |
|
����ʽ |
��Ԫ�ط��ű�ʾ���ʵķ������ |
CH4��C3H6 |
|
���ʽ (ʵ��ʽ) |
��ʾ������ɵĸ�Ԫ��ԭ�ӵ���������� |
��ϩ���ʽΪCH2��C6H12O6���ʽΪCH2O |
|
����ʽ |
��С�ڵ���������ű�ʾԭ���������ӵijɼ���� |
|
|
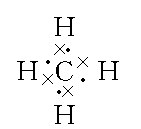
�ṹʽ |
�ö�������������ʾ1�����ۼ�����������(����)������(˫��)�����ԡ�(����)������ԭ���������� |
CHHCHH |
|
�ṹ |
||
|
��ʽ |
����ʾ����������������ʡ�ԣ�����̼ԭ������������ԭ��д�����Աߣ������½�ע������� |
|
|
����ʾ̼̼˫����̼̼���������������ԡ�����ʡ�� |
||
|
��ȩ��(COH)���Ȼ�(COOH)�ɼ���CHO����COOH |
CH3CHCH2�� |
|
|
CH3CH2OH�� |
||
|
HCOCOOH |
||
|
����ʽ |
����һ��ʡȥ̼��Ԫ�صķ��ţ�ֻҪ���ʾ��̼̼���Լ���̼ԭ�������Ļ��� |
|
|
��ͼʽ�е�ÿ���յ���յ����ʾһ��̼ԭ�ӣ�ÿ��̼ԭ�Ӷ��γ��ĸ����ۼ������������ԭ�Ӳ��� |
CH3CHCHCHCH3CH3 |
|
|
�ɱ�ʾΪ�� |
||
|
|
||
|
��� |
||
|
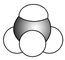
ģ�� |
С���ʾԭ�ӣ��̹���ʾ�ۼ� |
|
|
���� |
||
|
ģ�� |
�ò�ͬ�����С���ʾ��ͬԭ�ӵĴ�С |
|