1. 水是一种战略性经济资源,下列物质对水质不会产生严重污染的是
A.CH3OH B.SO2 C.HgCl2 D.CO2
2. 以下关于物质分类的说法正确的是
①液氨和液氯都是纯净物;②纯碱和熟石灰都是碱;③冰和干冰既是纯净物又是化合物;④高氯酸和硫酸钡都是强电解质;⑤Na2S、Na2O2、Na2SiO3都是钠盐
A.①②③ B.①②⑤ C.①③④ D.①③⑤
3. 下列有关化学用语表示正确的是
A.CaH2的电子式:[H:]-Ca2+[:H]- B.Cl-的结构示意图: 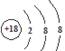
C.质子数为92、中子数为146的U原子:![]()
![]()
D.CH
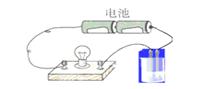 4. 用右图所示的装置分别进行如下导电性实验,小灯泡的亮度比反应前明显减弱的是
4. 用右图所示的装置分别进行如下导电性实验,小灯泡的亮度比反应前明显减弱的是
A.向亚硫酸钠溶液中通入氯气
B.向硝酸银溶液中通入少量氯化氢
C.向氢碘酸饱和溶液中通入少量氧气
D.向氢氧化钠溶液中通入少量氯气
5. 石墨烯是从石墨中剥离出来的,其结构如图所示。单层的石墨烯其厚度只有一个碳原子厚,被证实是世界上已经发现的最薄、最坚硬的物质,可制成电阻率最小的纳米材料。下列关于石墨烯的说法正确的是
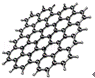
A.石墨烯与金刚石互为同位素
B.从石墨中剥离得石墨烯需克服范德华力
C.石墨烯是高分子化合物
D.制成的纳米材料微粒直径在1nm~100nm,因此石墨烯纳米材料属于胶体
6. 下列实验操作或现象解释不正确的是
A. 进行焰色反应时,必须用稀硫酸洗涤并灼烧铂丝,然后再进行实验
B. 分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
C. 读取滴定管内液体体积时,俯视读数导致读数偏小
D. 利用一束强光照射明矾水溶液,产生光亮的“通路”,说明明矾一定发生了水解
7. 动车组列车,****时速可达
A.铁路勘探时常用太阳能电池提供能量,太阳能电池是原电池
B.铁轨焊接时常用到铝热反应,铝热反应中放出大量的热足以使铁熔化
C.铁元素在周期表中位于第四周期ⅡB族
D.工业上铁、铝的冶炼均采用热还原法
8.下列各组物质充分反应后,只能得到一种气体的是
A.锌和浓硫酸共热 B.Na2O2与足量的稀硫酸反应
C.木炭和浓硫酸共热 D.足量的铜跟一定量的浓硝酸反应
9. 在下列变化①工业制盐酸 ②工业制漂粉精 ③实验室制氯气中,按氯元素被氧化、被还原、既被氧化又被还原的顺序排列,正确的是
A.①②③ B.②①③ C.③①② D. ①③②
10.短周期元素M、X、Y、Z,在周期表中所处的位置如图所示。M元素原子的最外层电子数为其次外层电子数的2倍。X、Y、Z三种元素原子质子数之和为32。则下列说法正确的是
|
X |
Z | |
|
Y |
A.元素M与氢元素组成化合物一定是正四面体型分子
B.X、Y两种元素的气态氢化物均能与它们对应的****价氧化物的水化物发生反应,且反应类型相同
C.X、Z两种元素的氢化物相互反应的产物是共价化合物
D.四种元素形成的气态氢化物中,Z元素形成的氢化物热稳定性****
11.氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是
A.AlON和石英的化学键类型相同 B.AlON和石英晶体类型相同
C.AlON中N元素的化合价为-1 D.电解熔融AlON或电解熔融Al2O3都能得到Al
12.设NA 为阿伏加德罗常数的值。下列说法正确的是
A.3.4gNH3中含N—H键数目为0.2 NA
B.标准状况下,体积相同的两种气体的分子数一定相同
C.标准状况下,
D.
13.铁铜合金中逐滴加入稀硝酸的过程中,下列离子方程式较难发生的是
A.Fe + 4H++ NO3-→ Fe3++ NO↑+ 2H2O
B.3Fe + 8H++ 2 NO3-→ 3Fe2++ 2NO↑+ 4H2O
C.3Cu + 8H++ 2 NO3-→ 3Cu2++ 2NO↑+ 4H2O
D.3Fe2+ + 4H+ + NO3-→ 3Fe3+ + NO↑ + 2H2O
14.已知二氯化二硫(S2Cl2)的结构式为Cl-S-S-Cl,它易与水反应2S2Cl2+2H2O→4HCl+SO2↑+3S↓。在该反应中
A.S2Cl2既作氧化剂又作还原剂 B.氧化产物与还原产物物质的量比为3:1
C.每生成
15.下列离子或分子在溶液中能大量共存,但通入NO2后不能大量共存,且不会生成沉淀的一组是
A.K+、Na+、NO3-、SiO32- B.Al3+、K+、SO42-、S2-
C.Ag+、Na+、NH3·H2O、NO3- D.Cu2+、Fe2+、Cl-、SO42-
16. 由下列实验事实所得出的相应结论的因果关系正确的是
|
实验事实 |
结论 | |
|
A |
KClO3和SO3溶于水后能导电 |
KClO3和SO3为电解质 |
|
B |
SO2通入硝酸钡溶液出现白色沉淀 |
BaSO3不溶于强酸 |
|
C |
将CO2通入NaAlO2溶液会产生白色沉淀 |
结合H+的能力:HCO<AlO |
|
D |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
17. 依据物质的相关数据,可以推断物质的结构和性质。下列利用物质的相关数据作出的相应推断不合理的是
A.依据元素的原子序数,推断该元素原子的核外电子数
B.依据物质相对分子质量,推断物质熔、沸点的高低
C.依据气体的摩尔质量,推断相同状态下不同气体密度的大小
D.依据液体物质的沸点,推断将两种互溶液态混合物用蒸馏法分离的可行性
18. 莫尔盐[(NH4)2Fe(SO4)2•6H2O]溶液经常用于定量滴定实验,下列有关说法正确的是( )
A.配制0.1mol·L-1莫尔盐溶液500mL,需莫尔盐
B.可与含Fe2+、HClO、H+、Cl﹣微粒的溶液大量共存
C.加入过量Ba(OH)2溶液发生反应:2Ba2++2SO42﹣+Fe2++2OH﹣=2BaSO4↓+Fe(OH)2↓
D.取样,加入浓NaOH溶液并加热,出现可让蓝色石蕊试纸变红的气体,证明含NH4+
19. 下列离子方程式中正确的是
A.NH4HSO4溶液中加入少量NaOH稀溶液:NH4+ + OH- = NH3·H2O
B.Ca(ClO)2溶液中通入过量的二氧化硫气体:ClO- + SO2 + H2O=HClO + HSO3-
C.酸性高锰酸钾溶液中滴入少量过氧化氢:2MnO4- +7H2O2+6H+ =2Mn2+ + 6O2↑ + 10H2O
D.为缓解胃酸过多,服含NaHCO3的抗酸药:HCO3—+H+=H2O+CO2↑
20.下表为五种短周期元素的部分性质。
|
元素代号 |
X |
Y |
Z |
Q |
R |
|
原子半径/10- |
0.37 |
0.66 |
0.70 |
0.88 |
0.99 |
|
主要化合价 |
+1 |
-2 |
+5、-3 |
+3 |
+7、-1 |
下列有关说法正确的是
A.元素X、Y、Z形成的化合物一定是离子化合物
B.X元素和R元素形成的化合物XR是18电子的分子
C.化合物QR3分子中各原子均满足8电子稳定结构
D.元素Z的氧化物对应水化物一定为强酸
21. 下列有关说法正确的是
A.分子晶体中共价键越强,熔沸点越高
B.只含共价键的物质,一定是共价化合物
C.HF的分子间作用力大于HCl,故HF比HCl更稳定
D.分子晶体中,可能不存在共价键,但一定存在分子间作用力
22.下列实验操作、现象和结论均正确的是
|
选项 |
实验操作 |
现象 |
结论 |
|
A |
SO2通入溴水中 |
溶液褪色 |
SO2有漂白性 |
|
B |
将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 |
溶液变红 |
Fe(NO3)2样品已氧化变质 |
|
C |
取等物质的量的两种金属单质X、Y,分别与足量的盐酸反应 |
X产生氢气的体积比Y多 |
金属性:X>Y |
|
D |
分别向0.1 mol·L-1醋酸和饱和硼酸溶液中滴加0.1mol·L-1Na2CO3溶液 |
醋酸中有气泡产生,硼酸中没有气泡产生 |
酸性:醋酸>碳酸>硼酸 |
23.下列反应与Na2O2+SO2=Na2SO4相比较,Na2O2的作用相同的是
A.2Na2O2+2CO2═2Na2CO3+O2 B.2Na2O2+2SO3═2 Na2SO4+O2
C.3Na2O2+Cr2O3═2Na2CrO4+Na2O D. Na2O2+H2SO4═Na2SO4+H2O2
24.2005年有科学家在《Science》上发表论文,宣布发现铝的超原子结构Al13和Al14,并在质谱仪检测到稳定的Al13- ……等。Al13、Al14的性质很像现行周期表中某些主族元素,已知当这类超原子具有40个价电子时最稳定(价电子指最外层电子)。下列说法不正确的是
A.Al13与卤素原子(ⅦA族)性质相似,能形成稳定的Al13-
B.Al14与HI反应的化学方程式为:Al14+2HI═Al14I2+H2↑
C.Al13超原子中Al原子间是通过离子键结合的
D.Al14超原子共有42个价电子,容易失去2个电子形成稳定的Al142+
25. 将a g二氧化锰粉末加入b mol/L的浓盐酸c L中加热****溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是
A.可以收集到氯气![]() L B.NA可表示为:
L B.NA可表示为:![]()
C.反应后溶液中的Cl―数目为:![]() D.反应后溶液中的H+数目为:
D.反应后溶液中的H+数目为:![]()
