“ΜΓΔ―Γ‘ώΧβΘ®ΟΩ–ΓΧβ÷Μ”–“ΜΗω’ΐ»Ζ¥πΑΗΘ§ΟΩΧβ3Ζ÷Θ§Ι≤48Ζ÷Θ©
1Θ°‘Ύ ΔΖ≈≈®ΝρΥαΒΡ ‘ΦΝΤΩΒΡ±ξ«©…œ”Π”Γ”–œ¬Ν–Ψ· Ψ±ξΦ«÷–ΒΡΘ®ΓΓΓΓΘ©
AΘ°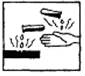 BΘ°
BΘ° CΘ°
CΘ° DΘ°
DΘ°
2Θ°œ¬Ν– Β―ι≤ΌΉς÷–¥μΈσΒΡ «Θ®ΓΓΓΓΘ©
AΘ°Ζ÷“Κ ±Θ§Ζ÷“Κ¬©ΕΖœ¬≤ψ“ΚΧε¥”œ¬ΩΎΖ≈≥ωΘ§…œ≤ψ“ΚΧε¥”…œΩΎΒΙ≥ω
BΘ°’τΝσ ±Θ§”Π ΙΈ¬Ε»ΦΤΥ°“χ«ρΩΩΫϋ’τΝσ…’ΤΩ÷ßΙήΩΎ
CΘ°’τΖΔΫαΨß ±”ΠΫΪ»ή“Κ’τΗ…
DΘ°≥ΤΝΩ ±Θ§≥ΤΝΩΈοΖ≈‘Ύ≥ΤΝΩ÷Ϋ…œΘ§÷Ο”ΎΆ–≈ΧΧλΤΫΒΡΉσ≈ΧΘ§μά¬κΖ≈‘ΎΆ–≈ΧΧλΤΫΒΡ”“≈Χ÷–
3Θ°œ¬Ν– Β―ι≤ΌΉς÷–Θ§≤ΜΡή”Ο”ΎΈο÷ Ζ÷άκΒΡ «Θ®ΓΓΓΓΘ©
AΘ° BΘ°
BΘ°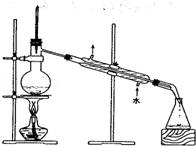 CΘ°
CΘ°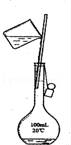 DΘ°
DΘ°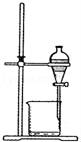
4Θ°KCl»ή“Κ÷–Μλ”–…ΌΝΩΒΡCuSO4Θ§»τΦ”»κ“Μ÷÷ ‘ΦΝΡή≥ΐ»ΞCuSO4Θ°ΗΟ ‘ΦΝΈΣΘ®ΓΓΓΓΘ©
AΘ°BaΘ®OHΘ©2 BΘ°NaOH CΘ°BaCl2 DΘ°AgNO3
5Θ°œ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°ΡΠΕϊ «Ω…“‘Α―Έο÷ ΒΡ÷ ΝΩ”κΈΔΙέΝΘΉ” ΐΝΣœΒΤπά¥ΒΡ“ΜΗωΜυ±ΨΈοάμΝΩ
BΘ°0.012 kg 12C÷–ΥυΚ§ΒΡΧΦ‘≠Ή” ΐΈΣNA
CΘ°Έο÷ ΒΡΡΠΕϊ÷ ΝΩΒ»”ΎΤδœύΕ‘Ζ÷Ή”Θ®‘≠Ή”Θ©÷ ΝΩ
DΘ°1mol»ΈΚΈΈο÷ ΕΦΚ§”–‘Φ6.02ΓΝ1023Ηω‘≠Ή”
6Θ°”ΟNA±μ ΨΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΘ§œ¬Ν––π ω’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°≥ΘΈ¬≥Θ―Ιœ¬Θ§22.4 L CCl4ΓΔCO2Κ§”–ΒΡΖ÷Ή” ΐΈΣNA
BΘ°Ά®≥ΘΉ¥Ωωœ¬Θ§NAΗωCO2Ζ÷Ή”’Φ”–ΒΡΧεΜΐ‘ΦΈΣ22.4 L
CΘ°≥ΘΈ¬≥Θ―Ιœ¬Θ§1.06 g Na2CO3Κ§”–ΒΡNa+άκΉ” ΐΈΣ0.02NA
DΘ°Έο÷ ΒΡΝΩ≈®Ε»ΈΣ0.5 mol/LΒΡMgCl2»ή“Κ÷–Θ§Κ§”–Cl©¹Ηω ΐΈΣNA
7Θ°1g N2÷–Κ§”–xΗω‘≠Ή”Θ§‘ρΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷Β «Θ®ΓΓΓΓΘ©
AΘ°![]() mol©¹1 BΘ°
mol©¹1 BΘ°![]() mol©¹1 CΘ°14x mol©¹1 DΘ°28x mol
mol©¹1 CΘ°14x mol©¹1 DΘ°28x mol
8Θ°1.0mol•L©¹1ΒΡNaCl»ή“Κ±μ ΨΘ®ΓΓΓΓΘ©
AΘ°»ή“Κ÷–Κ§”–1mol NaCl BΘ°1mol NaCl »ή”Ύ1LΥ°÷–
CΘ°58.5g NaCl»ή”Ύ941.5gΥ°÷– DΘ°1L»ή“ΚάοΚ§”–NaCl 58.5g
9Θ°œ¬Ν–»ή“Κ¬»άκΉ”ΒΡΈο÷ ΒΡΝΩ≈®Ε»”κ50mL 1mol•L©¹1¬»Μ·¬Ν»ή“Κ÷–¬»άκΉ”ΒΡΈο÷ ΒΡΝΩ≈®Ε»œύΒ»ΒΡ «Θ®ΓΓΓΓΘ©
AΘ°150 mL 1 mol•L©¹1¬»Μ·ΡΤ»ή“Κ
BΘ°75 mL 1.5 mol•L©¹1¬»Μ·ΗΤ»ή“Κ
CΘ°150 mL 2 mol•L©¹1¬»Μ·ΦΊ»ή“Κ
DΘ°50 mL 3 mol•L©¹1¬»Μ·ΟΨ»ή“Κ
10Θ°“Σ≈δ÷Τ≈®Ε»‘ΦΈΣ2mol•L©¹1NaOH»ή“Κ100mLΘ§œ¬Οφ≤ΌΉς’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°≥Τ»Γ8gNaOHΙΧΧεΘ§Ζ≈»κ100mL…’±≠÷–Θ§”Ο100mLΝΩΆ≤ΝΩ»Γ100mL’τΝσΥ°Θ§Φ”»κ…’±≠÷–Θ§Ά§ ±≤ΜΕœΫΝΑη÷ΝΙΧΧε»ήΫβ
BΘ°≥Τ»Γ8gNaOHΙΧΧεΘ§Ζ≈»κ100mLΝΩΆ≤÷–Θ§±ΏΫΝΑηΘ§±ψ¬ΐ¬ΐΦ”»κ’τΝσΥ°Θ§¥ΐΙΧΧε****»ήΫβΚσ”Ο’τΝσΥ°œΓ Ά÷Ν100mL
CΘ°≥Τ»Γ8gNaOHΙΧΧεΘ§Ζ≈»κ100mL»ίΝΩΤΩ÷–Θ§Φ”»κ ΝΩ’τΝσΥ°Θ§’ώΒ¥»ίΝΩΤΩ ΙΙΧΧε»ήΫβΘ§‘ΌΦ”Υ°ΒΫΩΧΕ»Θ§Η«ΚΟΤΩ»ϊΘ§Ζ¥Η¥“Γ‘»
DΘ°”Ο100mLΝΩΆ≤ΝΩ»Γ40mL5mol•L©¹1NaOH»ή“ΚΘ§ΒΙ»κ250mL…’±≠÷–Θ§‘Ό”ΟΆ§“ΜΝΩΆ≤»Γ60mL’τΝσΥ°Θ§≤ΜΕœΫΝΑηœ¬Θ§¬ΐ¬ΐΒΙ»κ…’±≠
11Θ°»ή“ΚΓΔΫΚΧεΚΆΉ«“Κ’β»ΐ÷÷Ζ÷…ΔœΒΒΡΗυ±Ψ«χ±π «Θ®ΓΓΓΓΘ©
AΘ°ΆβΙέ BΘ°Ζ÷…Δ÷ ΝΘΉ”ΒΡ¥σ–Γ
CΘ° «ΖώΡήΆ®Ιΐ¬Υ÷Ϋ DΘ° «Ζώ”–ΕΓ¥οΕϊ–ß”Π
12Θ°Β±“Μ χΙβΆ®Ιΐœ¬Ν–ΗςάύΖ÷…ΔœΒΘ§ΡήΙέ≤λΒΫΕΓ¥οΕϊ–ß”ΠΒΡ «Θ®ΓΓΓΓΘ©
ΔΌΉ«“Κ ΔΎ»ι“Κ Δέ»ή“Κ Δή―Χ ΔίΈμ Δό«β―θΜ·ΧζΫΚΧεΘ°
AΘ°÷Μ”–Δό BΘ°ΔήΔίΔό CΘ°ΔΌΔέΔί DΘ°»Ϊ≤Ω
13Θ°œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°“ΚΧ§HClΙΧΧεNaClΨυ≤ΜΒΦΒγΘ§Υυ“‘HClΓΔNaCl Ψυ «Ζ«ΒγΫβ÷
BΘ°NH3ΓΔCO2ΒΡΥ°»ή“ΚΨυΒΦΒγΘ§Υυ“‘NH3ΓΔCO2Ψυ «ΒγΫβ÷
CΘ°Ά≠ ·ΡΪΨυΒΦΒγΘ§Υυ“‘ΥϋΟ«Ψυ «ΒγΫβ÷
DΘ°’αΧ«ΓΔΨΤΨΪ‘ΎΥ°»ή“ΚΚΆ»έ»ΎΉ¥Χ§œ¬Ψυ≤ΜΒΦΒγΘ§Υυ“‘ΥϋΟ«Ψυ «Ζ«ΒγΫβ÷
14Θ°œ¬Ν–ΒγάκΖΫ≥Χ Ϋ÷–’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°Al2Θ®SO4Θ©3®T2Al3++3SO42©¹ BΘ°FeCl2®TFe2++3Cl©¹
CΘ°H2SO4®TH2++SO42©¹ DΘ°CaΘ®OHΘ©2®TCa2++2Θ®OH©¹Θ©
15Θ°œ¬Ν–άκΉ”ΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°Ά≠”κœθΥα“χ»ή“ΚΖ¥”ΠΘΚCu+Ag+=Cu2++Ag
BΘ°ΝρΥα”κ«β―θΜ·±Β»ή“ΚΖ¥”ΠΘΚOH©¹+Ba2++SO42©¹+H+=BaSO4Γΐ+H2O
CΘ°ΧΦΥαΗΤΚΆ―ΈΥαΖ¥”ΠΘΚCO32©¹+2H+=CO2Γϋ+H2O
DΘ°ΝρΥαΆ≠”κ«β―θΜ·±Β»ή“ΚΖ¥”ΠΘΚCu2++SO42©¹+Ba2++2OH©¹=BaSO4Γΐ+CuΘ®OHΘ©2Γΐ
16Θ°200mlFe2Θ®SO4Θ©3»ή“Κ÷–Κ§Fe3+56gΘ§»ή“Κ÷–SO42©¹ΒΡΈο÷ ΒΡΝΩ≈®Ε» «Θ®ΓΓΓΓΘ©
AΘ°5mol/L BΘ°7.5 mol/L CΘ°10 mol/L DΘ°2.5 mol/L
ΓΓ
ΕΰΘ°Ζ«―Γ‘ώΧβΘ®Ι≤5ΧβΘ©
17Θ°”–“‘œ¬ΦΗ÷÷Έο÷ ΘΚΔΌΗ…‘οΒΡ ≥―ΈΨßΧε ΔΎ““¥Φ ΔέΥ°“χ Δή’αΧ« Δί±υ¥ΉΥαΘ®¥Ω¥ΉΥαΨßΧεΘ© ΔόKNO3»ή“ΚΘ° ΧνΩ’ΜΊ¥πΘ®Χν–ρΚ≈Θ©ΘΚ
Θ®1Θ©“‘…œΈο÷ Ω…“‘ΒΦΒγΒΡ «ΓΓΓΓΘΜ
Θ®2Θ©“‘…œΈο÷ ÷– τ”ΎΒγΫβ÷ ΒΡ «ΓΓΓΓΘΜ
Θ®3Θ©“‘…œΈο÷ ÷– τ”ΎΖ«ΒγΫβ÷ ΒΡ «ΓΓΓΓΘ°
18Θ°œ÷”–mΩΥΡ≥ΤχΧεΘ§Υϋ”…ΥΪ‘≠Ή”Ζ÷Ή”ΙΙ≥…Θ§ΥϋΒΡΡΠΕϊ÷ ΝΩΈΣM g•mol©¹1Θ°»τΑΔΖϋΦ”Β¬¬ό≥Θ ΐ”ΟNA±μ ΨΘ§‘ρΘΚΗΟΤχΧεΥυΚ§‘≠Ή”Ήή ΐΈΣΓΓΓΓΗωΘΜΗΟΤχΧε‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐΈΣΓΓΓΓLΘΜΗΟΤχΧε»ή”ΎΥ°Κσ–Έ≥…V L»ή“ΚΘ§Τδ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣΓΓΓΓΘ°
19Θ°100mL 1mol•L©¹1Al2Θ®SO4Θ©3»ή“Κ÷–Κ§SO42©¹άκΉ”ΓΓΓΓΗωΘ§Κ§Al3+άκΉ”ΓΓΓΓmolΘ°
20Θ°0.6mol O2”κ0.4mol O3÷ ΝΩ÷°±»ΈΣΓΓΓΓΘ§Ζ÷Ή”Ηω ΐ÷°±»ΈΣΓΓΓΓΘ§‘≠Ή”Ηω ΐ÷°±»ΓΓΓΓΘ§ΥϋΟ«‘ΎΆ§Έ¬Ά§―Ιœ¬ΒΡΧεΜΐ±» «ΓΓΓΓΘ°
21Θ°ΟςΖ·ΒΡ÷ς“Σ≥…Ζ÷ΈΣKAlΘ®SO4Θ©2•12H2OΘ°
Θ®1Θ©Al‘≠Ή”ΒΡΫαΙΙ Ψ“βΆΦΓΓΓΓΘ°
Θ®2Θ©KAlΘ®SO4Θ©2•12H2O‘ΎΥ°÷–ΒΡΒγάκΖΫ≥Χ ΫΘΚΓΓΓΓΘ°
Θ®3Θ©ΟςΖ·»ή”ΎΥ°–Έ≥…AlΘ®OHΘ©3ΫΚΧεΘ§AlΘ®OHΘ©3ΫΚΧεΖ÷…Δ÷ ΝΘΉ”÷±ΨΕΫι”ΎΓΓΓΓ÷°ΦδΘ§«χ±πAlΘ®OHΘ©3ΫΚΧε”κAlCl3»ή“ΚΒΡ Β―ιΖΫΖ® «ΓΓΓΓΘ°
22Θ°Ρ≥ΩΈΆβ―–ΨΩ–‘―ßœΑ–ΓΉιΡβ”Ο¥÷―ΈΘ®Κ§”–…ΌΝΩ‘”÷ Αϋά®ΘΚΡύ…≥ΓΔCaCl2ΓΔMgCl2ΓΔNa2SO4Ψ≠Χα¥ΩΚσΘ§≈δ÷Τ0.4mol/L 450mL NaCl»ή“ΚΘ°ΥϊΟ«…ηΦΤ≤Δ Β ©ΝΥ»γœ¬ Β―ιΘ§«κΗυΨί“――ßΙΐΒΡ÷Σ ΕΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©»Γ“ΜΕ®ΝΩΒΡ¥÷―Έ÷Ο”Ύ…’±≠÷–Φ”Υ°»ήΫβΘ§ΥυΦ”ΒΡΥ°ΝΩ”ΠΈΣΘΚΓΓΓΓΘ®Χν―ΓœνΘ©
AΘ°ΕύΦ”Υ°≈δ≥…ΫœœΓΒΡ»ή“Κ BΘ°Φ”»κ ΝΩΒΡΥ°÷ΝΡή»ήΫβΒΡΙΧΧε»ήΫβΦ¥÷Ι
Θ®2Θ©ΫΪΘ®1Θ©÷–≈δ÷ΤΒΡ¥÷―Έ–ϋΉ«“ΚΙΐ¬ΥΚσ»Γ¬Υ“ΚΦ”»κΙΐΝΩΒΡ≥ΐ‘” ‘ΦΝΘ§“―÷ΣΘΚ
ΔΌNa2CO3»ή“ΚΔΎKOH»ή“Κ ΔέAgNO3»ή“Κ ΔήNaOH»ή“ΚΔίNaHCO3»ή“Κ
ΔόBaCl2»ή“ΚΘ§¥”÷–―Γ‘ώ’ΐ»ΖΒΡ≥ΐ‘” ‘ΦΝΚΆΦ”»κΒΡΥ≥–ρ”ΠΈΣΘΚΓΓΓΓΘ°
AΘ°ΔΌΔΎΔέBΘ°ΔΎΔόΔίCΘ°ΔήΔόΔΌDΘ°ΔΌΔήΔόEΘ°ΔόΔΌΔήFΘ°ΔόΔΎΔί
Θ®3Θ©ΫΪΥυΒΟΒΡ–ϋΉ«“ΚΨ≠Ιΐ¬ΥΚσ»Γ¬Υ“ΚΦ”»κΉψΝΩΒΡ―ΈΥαΘ§≥δΖ÷Ζ¥”ΠΚσΕ‘ΜλΚœ»ή“ΚΫχ––’τΖΔΓΔΙΐ¬ΥΓΔœ¥Β”ΓΔΗ…‘ο≤ΌΉςΘ§ΒΟΒΫ¥ΩΨΜΒΡNaClΙΧΧεΘ§«κΟη ω‘Ύ’τΖΔ≤ΌΉςΙΐ≥Χ÷–≤ΘΝßΑτΒΡΉς”ΟΘΚΓΓΓΓΘ°
Θ®4Θ©άϊ”ΟΘ®3Θ©÷–ΥυΒΟΒΡNaClΙΧΧεΥυ–η»ή“ΚΘ°‘ΎΆ–≈ΧΧλΤΫ…œ≥ΤΝΩΓΓΓΓg NaClΙΧΧεΘ°
≈δ÷ΤΙΐ≥Χ÷––η Ι”ΟΒΡ≤ΘΝß“«Τς”–ΘΚ…’±≠ΓΔ≤ΘΝßΑτΓΔΓΓΓΓΚΆΓΓΓΓΘ°
Θ®5Θ©≈δ÷ΤΫα χΚσΆ§―ßΟ«Ε‘ Β―ι÷–≥ωœ÷ΒΡΡ≥–©¥μΈσ≤ΌΉςΘ§Ε‘Ήν÷’≈δ÷ΤΒΡ»ή“Κ≈®Ε»ΒΡ”ΑœλΫχ––ΝΥΖ÷ΈωΘ§‘ρœ¬Ν–¥μΈσ≤ΌΉςΜαΒΦ÷¬Ήν÷’≈δ÷Τ»ή“Κ÷–NaClΒΡ≈®Ε»œύ±»0.4mol/LΒΡΤΪ≤ν «ΘΚΘ®ΧνΓΑΤΪ¥σΓ±ΓΔΓΑΤΪ–ΓΓ±ΓΔΓΑΈό”ΑœλΓ±Θ©
ΔΌ‘Ύ…œ ωΘ®2Θ©≤Ϋ÷–ΟΜ”– Ι”Ο―ΈΥα¥Πάμ¬Υ“ΚΘ§ΫαΙϊΜαΓΓΓΓΘΜ
ΔΎΟΜ”–Ε‘…’±≠ΚΆ≤ΘΝßΑτΫχ––œ¥Β”Θ§ΫαΙϊΜαΓΓΓΓΘΜ
ΔέΕ®»ί ±Η© ”ΑΦ“ΚΟφΘ§ΫαΙϊΜαΓΓΓΓΘΜ
Δή…œœ¬ΒΏΒΙ“Γ‘»Κσ“ΚΟφΒΆ”ΎΩΧΕ»œΏΘ§Έ¥ΦΑ ±Φ”Υ°÷ΝΩΧΕ»œΏΘ§ΫαΙϊΜαΓΓΓΓΘ°
―ß–ΘΉ…―·¥ΠΘΚ±ΘΕ® –ΨΚ–ψ«χΤΏ“Μ÷–¬Ζ1317Κ≈ Ή…―·ΒγΜΑΘΚ0312-4442550
¥όάœ ΠΘΚ15350617957Θ®Ά§ΈΔ–≈Θ© ΗΏάœ ΠΘΚ19213065640Θ®Ά§ΈΔ–≈Θ©
≥¬άœ ΠΘΚ13833233159Θ®Ά§ΈΔ–≈Θ© Ήφάœ ΠΘΚ19213027557Θ®Ά§ΈΔ–≈Θ©
ICP±ΗΑΗΚ≈ΘΚΦΫICP±Η17032056Κ≈-1
