课时训练1 物质的分类与转化
基础夯实
1.城市居民用天然气的主要成分为甲烷(CH4)。下列各组物质可与甲烷归为一类的是( )
A.H2、O2、N2 B.CO2、C2H6、C60
C.C2H6、C3H8、C4H10 D.乙醇、空气、汽油
答案:C
2.“长征二号”F火箭使用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作为推进剂,三子级则使用效能更高的液氢和液氧。下列有关说法正确的是( )
A.偏二甲肼和四氧化二氮都是氮的氧化物
B.液氢和液氧都是化合物
C.液氧是一种单质
D.四氧化二氮中氧原子与氮原子的个数比是1∶2
答案:C
3.实验室中的药品常按物质的性质、类别等有规律地摆放。现有部分药品按某种规律摆放在实验桌上,如下图所示。做“硫酸的性质”实验时,某同学取用Ba(OH)2溶液后,应把它放回的位置是( )
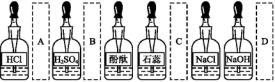
答案:D
4.在我们的日常生活中出现了“加碘食盐”“增铁酱油”“高钙牛奶”“富硒茶叶”“含氟牙膏”等商品。这里的碘、铁、钙、硒、氟应理解为( )
A.元素 B.单质 C.分子 D.氧化物
答案:A
解析:食品包装袋上关于食品的某些成分含量的说明均指元素含量。
5.下列物质属于酸性氧化物的是( )
A.Na2O B.CO C.CaO D.SO2
答案:D
解析:Na2O和CaO是碱性氧化物;CO虽然是非金属氧化物,但它不是酸性氧化物。
6.下列物质中属于纯净物的是( )
A.由同种元素组成的物质
B.具有固定熔沸点的物质
C.只由一种元素的阳离子和另一种元素的阴离子组成的物质
D.由两种元素组成的物质
答案:B
解析:由同种元素组成的物质可能为纯净物,也可能为混合物,如O2与O3,金刚石与石墨等,A错;由一种元素的阳离子和另一种元素的阴离子组成的物质也可能为混合物,如FeCl2与FeCl3相混合,C错。
7.下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是( )
A.空气、硫酸铜、硫酸
B.水、空气、纯碱
C.氧化铁、胆矾、熟石灰
D.硝酸、食盐水、烧碱
答案:D
解析:食盐水是氯化钠的水溶液,为混合物;烧碱是NaOH,为碱。
8.经测定一瓶气体中只含C和O两种元素,通常情况下这瓶气体不可能是( )(导学号52180045)
A.一种化合物
B.两种单质
C.两种化合物
D.一种单质和一种化合物的混合物
答案:B
解析:C和O两种元素可以形成的气体有CO、CO2、O2,所以不可能是两种单质。
9.符合图中阴影部分的物质是( )
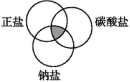
A.Na2CO3
B.Cu2(OH)2CO3
C.NaCl
D.NaHCO3
答案:A
解析:由题意知该物质是正盐,排除B、D。又是碳酸盐,可排除C,故选A。
10.初中阶段,我们已经学习了一些物质转化的知识。请举例说明下表所列物质的转化类型,并将你知道的其他的转化类型补充完成下表。
|
物质的转化类型 |
化学方程式 |
|
单质 |
C+O2 |
|
金属氧化物 |
CaO+H2O |
|
酸 |
Na2CO3+H2SO4 |
续表
|
物质的转化类型 |
化学方程式 |
|
碱 |
NaOH+HCl |
|
盐 |
AgNO3+NaCl |
11.下列物质:①Cu ②Na2CO3 ③NaHCO3
④Ca(OH)2 ⑤CH4 ⑥HNO3 ⑦KHSO4 ⑧CO2 ⑨生石灰,按要求填空(填序号):
(1)属于酸的是 ;
(2)属于碱的是 ;
(3)属于钠盐的是 ;
(4)属于酸式盐的是 ;
(5)属于单质的是 ;
(6)属于氧化物的是 ;
(7)属于有机物的是 。
答案:(1)⑥ (2)④ (3)②③ (4)③⑦ (5)① (6)⑧⑨ (7)⑤
能力提升
12.上海国际进出口食品展览会上展示了来自法国、德国、美国等国家的甜食、巧克力及休闲食品,其中有些包装食品的干燥剂的主要成分为生石灰(CaO)。(导学号52180046)
(1)生石灰属于哪种类别的物质? 。
(2)生石灰可作干燥剂的理由是 。
(3)生石灰还可以和哪些类别的物质发生化学反应?列举两例,并写出化学方程式。 。
(4)包装食品袋中的物质能否****、持续地作干燥剂?为什么? 。
答案:(1)既是金属氧化物,又是碱性氧化物
(2)CaO+H2O![]() Ca(OH)2
Ca(OH)2
(3)CaO还可与酸或酸性氧化物反应;CaO+2HCl![]() CaCl2+H2O,CaO+CO2
CaCl2+H2O,CaO+CO2![]() CaCO3
CaCO3
(4)不能。当CaO与水反应全部生成Ca(OH)2至表面呈黏稠状时,即失去干燥物质的能力
解析:(1)CaO按组成分类属于金属氧化物,按性质分类属于碱性氧化物。(3)CaO作为碱性氧化物具有碱性氧化物的通性,其干燥原理就是能吸收水并和H2O反应。(4)当CaO****与H2O反应后就不再具有干燥作用。
