4.前四周期原子序数依次增大的元素A、B、C、D、E中,A的基态原子核外3个能级上有电子,且每个能级上的电子数相等,B原子核外电子有7种不同的运动状态,C元素原子核外的M层中只有2对成对电子,D+与C2-的电子数相等,E元素位于元素周期表的ds区,且基态原子价电层电子均已成对。
回答下列问题:
(1)E2+的价层电子排布图为________________。
(2)五种元素中第一电离能最小的是________(填元素符号),CAB-离子中,A原子的杂化方式是________。
(3)AB-、D+和E2+三种离子组成的化学物质D2E(AB)4,其中化学键的类型有________________,该化合物中存在一个复杂离子,该离子的化学式为________,配位体是________。
(4)C和E两种元素组成的一种化合物的晶胞如图所示。
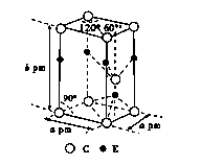
①该化合物的化学式为________,E的配位数为________,C采取________(填“简单立方”、“体心立方”、“六方最密”或“面心立方最密”)堆积;
②列式表示该晶体的密度:________g・cm-3。
 【答案】 (1)
【答案】 (1) ![]()
(2)K sp杂化
(3)共价键、配位键、离子键 Zn(CN)4]2- CN-
(4)①ZnS 4 六方最密
②3
5.已知:硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如图所示。请回答下列问题:
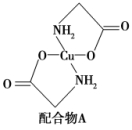
(1)Cu元素基态原子的外围电子排布式为________。
(2)元素C、N、O的第一电离能由大到小的顺序为________。
(3)配合物A中碳原子的轨道杂化类型为________。
(4)1 mol氨基乙酸钠(H2NCH2COONa)含有σ键的数目为________________。
(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:________(写化学式)。
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图。则该化合物的化学式是________。
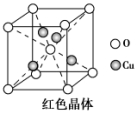
 【答案】 (1)3d104s1 (2)N>O>C
【答案】 (1)3d104s1 (2)N>O>C
(3)sp2、sp3 (4)8×6.02×1023
(5)N2O(或SCN-、N3等) (6)Cu2O
6.过渡元素Ti、Mn、Fe、Cu等可与C、H、O形成多种化合物。请回答下列问题:
(1)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Mn属于________区。
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti2+中电子占据的****能层符号为________,该能层具有的原子轨道数为________。BH4的立体构型是________。
(3)在Cu的催化作用下,乙醇可被空气中氧气氧化为乙醛,乙醛分子中碳原子的杂化方式是________,乙醛分子中HCO的键角________乙醇分子中HCO的键角(填“大于”、“等于”或“小于”)。
(4)电镀厂排放的废水中常含有剧毒的CN-,可在TiO2的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。
①H、C、N、O四种元素的电负性由小到大的顺序为________________。
②与CN-互为等电子体微粒的化学式为________(写出一种即可)
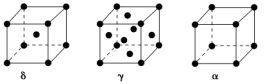
(5)单质铁有δ、γ、α三种同素异形体,三种晶胞中Fe原子的配位数之比为________,δ、γ、α三种晶胞的边长之比为________。
 【答案】 (1)d (2)M 9 正四面体形
【答案】 (1)d (2)M 9 正四面体形
(3)sp2、sp3 大于
(4)①H<C<N<O ②CO(或N2等)
(5)4∶6∶3 3∶∶1
7.氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有****的耐磨性。它们的晶体结构如下图所示。
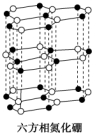
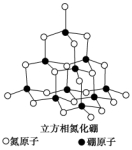
(1)基态硼原子的电子排布式为________________________________________________。
(2)关于这两种晶体的说法,正确的是________(填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为________________,其结构与石墨相似却不导电,原因是______________________________________________。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为________。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是____________________________________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有________ mol配位键。

【答案】 (1)1s22s22p1或He]2s22p1 (2)bc
(3)平面三角形 层状结构中没有自由移动的电子
(4)sp3 高温、高压 (5)2
8.铜是重要的金属,广泛应用于电气、机械制造、国防等领域,铜的化合物在科学研究和工农业生产中有许多用途。回答下列问题:
(1)Cu原子的价层电子排布式为________。
(2)CuSO4晶体中S原子的杂化方式为________,SO4的立体构型为________。
(3)向CuSO4溶液中加入过量氨水,可生成Cu(NH3)4]SO4,下列说法正确的是________。
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子立体构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4]SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4]SO4的组成元素中电负性****的是氮元素

【答案】 (1)3d104s1 (2)sp3 正四面体 (3)c