9.已知A、B、C、D、E、F、G七种元素,它们的原子序数依次增大。A在所有元素中原子半径最小;B原子核外电子有6种不同运动状态;D与C、E均相邻;A、D、E三种元素的原子序数之和为25;E2-和F+有相同的核外电子排布;G的质子数是25。请回答下列问题:
(1)写出元素G的基态原子外围电子排布式________;B、C、D三种元素分别形成的最简单氢化物的沸点****的是________(用化学式表示)。
(2)由上述元素中的两种元素组成的一种阴离子与D的一种同素异形体分子互为等电子体,该阴离子化学式为________。
(3)由上述元素组成的属于非极性分子且VSEPR为直线形的微粒的电子式________(任写一种)。
(4)M是由4个C原子组成的一种不稳定的多原子单质分子,M分子中C原子杂化方式为sp3杂化,M分子的立体构型为________。
(5)某一次性电池的比能量和可储存时间均比普通干电池优良,适用于大电流和连续放电,是民用电池的升级换代产品之一,它的负极材料是Zn,正极材料是G的一种常见氧化物,电解质是KOH。该电池的正极反应式为______________。
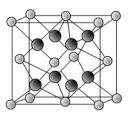
(6)由上述元素中电负性****的元素和第一电离能最小的元素形成的某化合物N的晶胞如右图所示。化合物N与氧化钙相比,晶格能较小的是______(填化学式)。已知该化合物的晶胞边长为a pm,则该化合物的密度为________g・cm-3(只要求列出算式,不必计算出数值,阿伏加德罗常数的数值为NA,1 pm=10-10cm)。

【答案】 (1)3d54s2 H2O
(2)NO2 (3) ![]() (或H∶C⋮⋮C∶H)
(或H∶C⋮⋮C∶H)
(4)正四面体
(5)MnO2+e-+H2O===MnOOH+OH-
(6)K2O NA×a3×10-30
10.下表为元素周期表的一部分,其中的编号代表所对应的元素。请回答下列问题: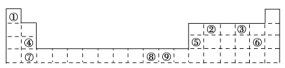
(1)⑨号元素的基态原子的价电子排布式是________,与其同周期,且基态原子的核外未成对电子数最多的元素是_______________________________(写出元素符号),②号元素基态原子的电子排布图为________。
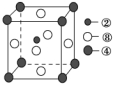
(2)①号与③号元素形成的含有18电子的物质为________(写出名称),②号与③号元素形成的,能造成温室效应的物质的立体构型为________。②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为________(用对应的元素符号表示),常温条件下丙烯是气态,而相对分子质量比丙烯小的甲醇,常温条件下却呈液态,出现这种现象的原因是______________________________
_________________________________________________________________________________________。
(3)①、②两种元素能形成多种平面形分子,其中有一种相对分子质量最小,有关该分子的说法中正确的是________。
a.该分子属于含有极性键的非极性分子
b.该分子含有4个σ键和1个π键
c.该分子中的②号原子采取sp2杂化
d.该物质易溶于水,并能和水反应得到酒精
(4)某元素的价电子排布式为nsnnpn+1,该元素可与元素①形成含有10个电子的分子X,将过量的X通入盛有硫酸铜溶液的试管里,产生的现象为_____________________________________________________。
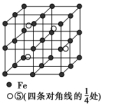
(5)若元素⑤与Fe元素形成的某种晶体如图所示。若晶胞的边长为a nm,则合金的密度为________g・cm-3。
 【答案】 (1)3d104s1 Cr
【答案】 (1)3d104s1 Cr
![]()
![]()
(2)过氧化氢 直线形 MgNi3C(或Ni3MgC)
甲醇分子间存在氢键,而丙烯分子间只有范德华力
(3)ac
(4)先产生蓝色沉淀,后沉淀消失,溶液变成深蓝色
(5)0.92/a3或5.56×1023/(a3NA)
11. A、B、C、D、E、F是周期表前四周期中的常见元素,其相关信息如下表:
|
元素 |
相关信息 |
|
A |
周期表中原子半径最小的元素 |
|
B |
元素的原子价电子排布为nsnnpn |
|
C |
基态原子L层电子数是K层电子数的3倍 |
|
D |
第三周期中第一电离能最小的元素 |
|
E |
地壳中含量最多的金属元素 |
|
F |
有多种化合价,其某种高价阳离子的价电子具有较稳定的半充满结构 |
(1)F位于元素周期表中位置是________,其基态原子核外价电子排布式为________。
(2)B的电负性比C的________(填“大”或“小”);B2A2分子中σ键与π键个数之比为________。
(3)写出E的单质与D的****价氧化物的水化物溶液反应的化学方程式:_________________________________________________________________。
(4)已知每5.4 gE可与F的低价氧化物反应,放出346.2 kJ的热量。请写出该反应的热化学方程式:_______________________________________________。
![]()
【答案】 (1)第四周期Ⅷ族 3d64s2
(2)小 3∶2
(3)2Al+2NaOH+2H2O===2NaAlO2+3H2↑
(4)2Al(s)+3FeO(s)===3Fe(s)+Al2O3(s)
ΔH=-3 462 kJ/mol
12.2013年诺贝尔化学奖授予三位美国科学家,以表彰他们如光合作用叶绿体光反应时酶中、生物固氮时固氮酶中)的化学反应。
(1)固氮酶有铁蛋白和钒铁蛋白两种,它们不仅能够催化N2还原成NH3,还能将环境底物乙炔催化还原成乙烯,下列说法正确的有________(不定项选择)。
a.C2H2、C2H4都是非极性分子
b.碳负离子CH3呈三角锥形
c.NO+电子式为∶N⋮⋮O∶]+
d.NH3沸点比N2高,主要是因为前者是极性分子
(2)钒可合成电池电极,也可人工合成二价钒(V)固氮酶(结构如图)
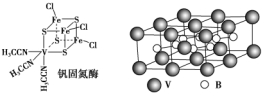
①V2+基态时核外电子排布式为______________________________________。
②钒固氮酶中钒的配位原子有________(写元素符号)。
③熔融空气电池钒硼晶体晶胞结构如图所示,该晶胞中含有钒原子数目为________。
(3)烟酰胺(结构简式如图)可用于合成光合辅酶NADPH,烟酰胺分子中氮原子的杂化轨道类型有________,1 mol该分子中含σ键的数目为___________________________________________________________。


【答案】 (1)abc
(2)①1s22s22p63s23p63d3或Ar]3d3 ②S、N ③4
(3)sp2、sp3 15NA(或15×6.02×1023)